





In einer komplexen Therapielandschaft eröffnen uns Biomarker ein tieferes Verständnis für Patientenpopulationen. Die Analyse von Biomarkern kann zu einem präziseren Patientenprofil beitragen und damit informierte Entscheidungen zu maßgeschneiderten Therapiestrategien unterstützen.


FGFR2b=fibroblast growth factor receptor 2b; HER2=human epidermal growth factor receptor 2b; MSI=microsatellite instability; PD-L1=programmed death-ligand 1.
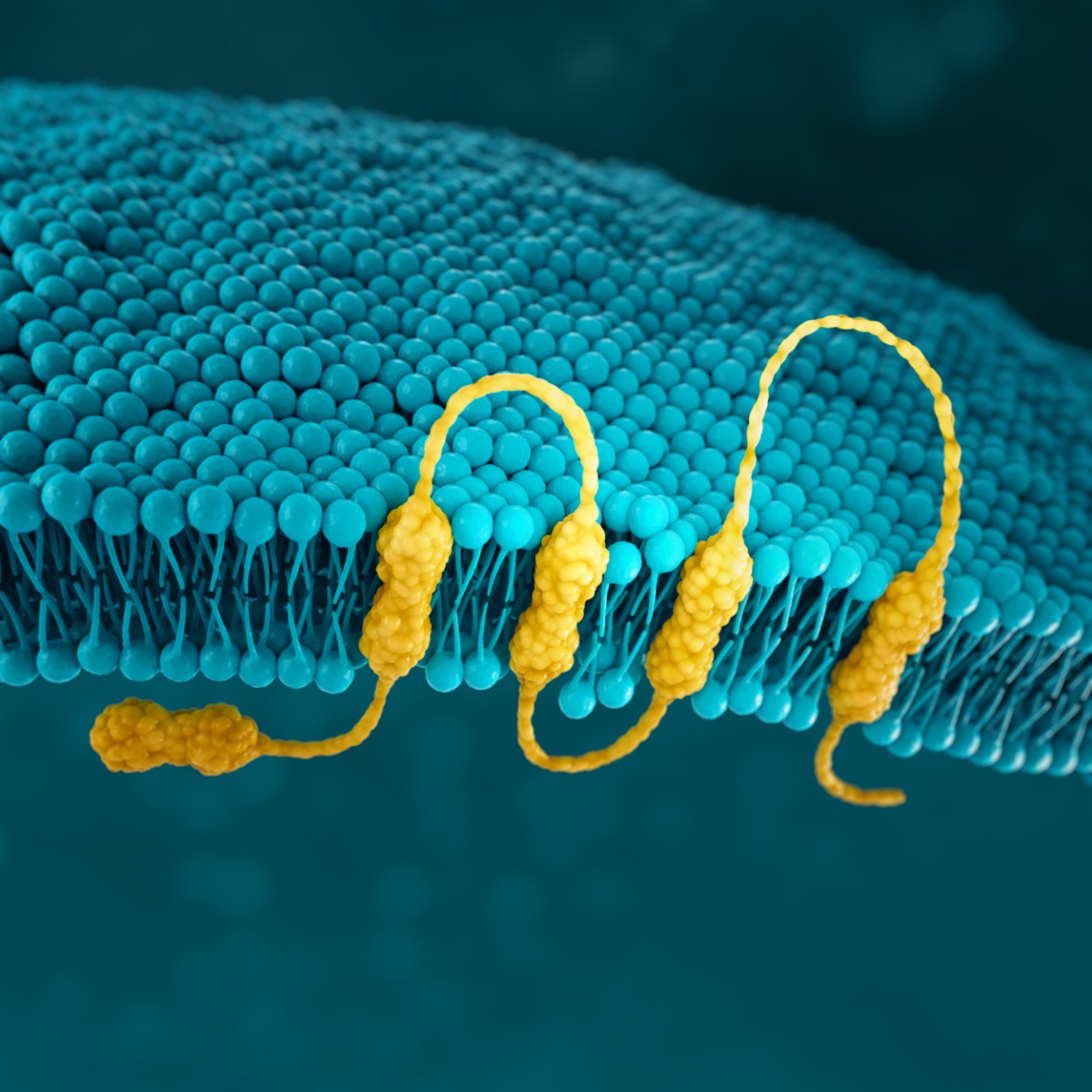
CLDN18.2
Claudine sind eine Familie von Transmembranproteinen.2,25
Claudine sind ein Hauptbestandteil von epithelialen und endothelialen Tight Junctions, die an der Steuerung des Molekülflusses zwischen Zellen beteiligt sind.2-4
Claudine kommen im gesamten Körper vor. Zwei Isoformen von Claudin 18 sind jedoch spezifisch für bestimmte Gewebe2,25:
Aus präklinischen Studien geht hervor, dass Claudin 18.2 im Zuge der Entstehung von Magentumoren eine erhöhte Exposition aufweist und dadurch potenziell zugänglicher für Antikörper werden kann.2,26,27
IN GESUNDEM
GEWEBE
UMSCHLOSSEN


In Magenepithelzellen ist Claudin 18.2 typischerweise im supramolekularen Komplex der Tight Junctions verborgen.2,4,27
Es reguliert die selektive Permeabilität und trägt zur Adhäsion zwischen den Epithelzellen bei.2-5
EXPONIERT IM
RAHMEN DER
TUMORGENESE


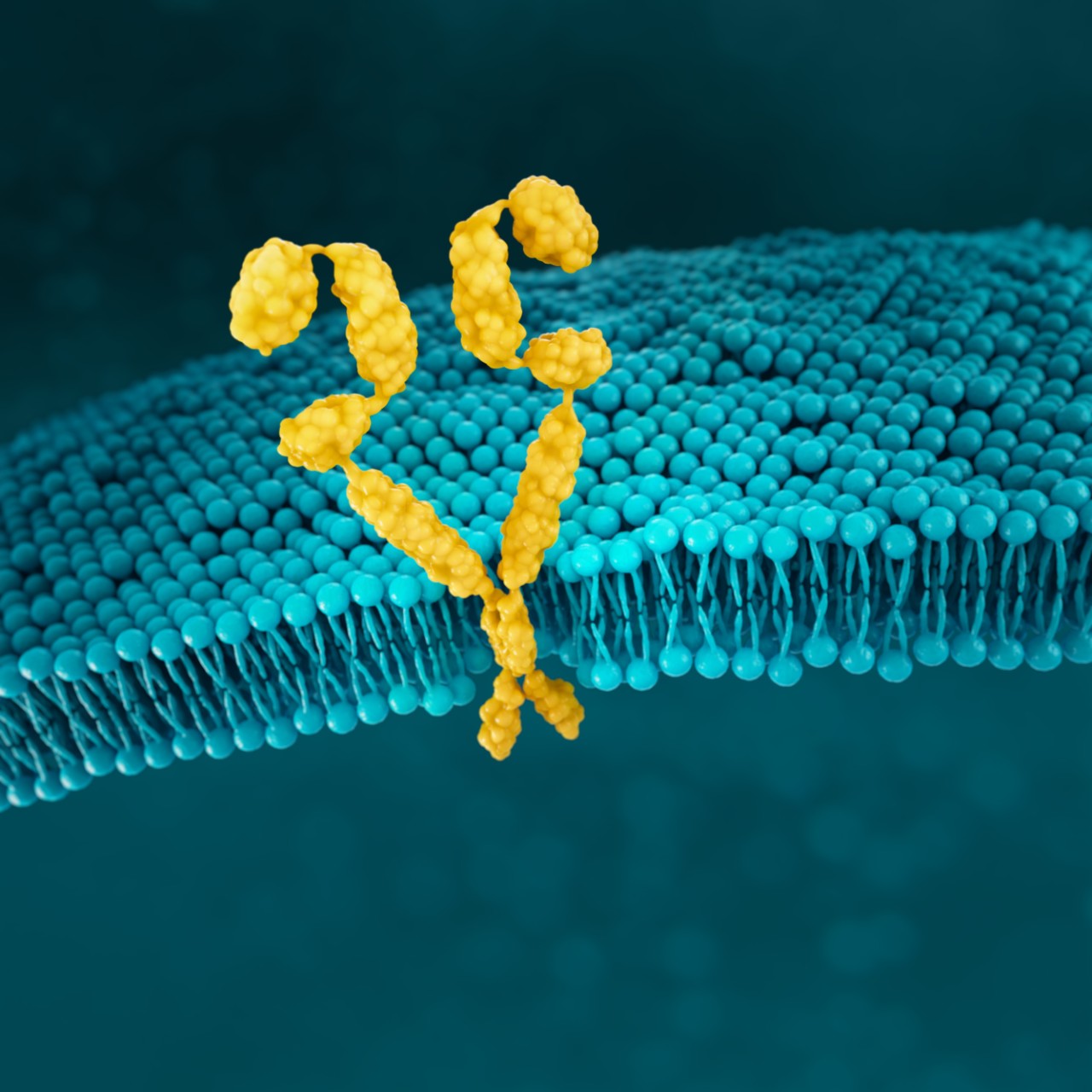
Die maligne Transformation der Magenepithelzellen führt zu
Polaritätsstörungen und Strukturverlust.26,27
Infolgedessen kann Claudin 18.2 auf diesen Zellen eine erhöhte Exposition aufweisen und für Antikörper zugänglicher werden.2,26,27
ERHALTEN WÄHREND DER TRANSFORMATION


Claudin 18.2 bleibt während der gesamten malignen Transformation sowohl im Primärtumor als auch in den Metastasen exponiert.2,26
Auch bei der Entwicklung von Tumoren in Ösophagus-, Pankreas-, Lungen- und Eierstockgewebe kann Claudin 18.2 exprimiert werden.2
Etwa 70 % aller Adenokarzinome des Magens/AEG exprimieren Claudin 18.2, wovon etwa die Hälfte eine hohe Expression von Claudin 18.2 (Claudin 18.2+) aufweisen.19


Eine Auswertung von Daten zur Ko-Expression von Claudin 18.2 und anderen Biomarkern ergab eine begrenzte Überschneidung.19








*In die Untersuchung wurden 350 kaukasische Patienten mit Adenokarzinom des Magens und AEG eingeschlossen, von denen 117 eine hohe Expression von Claudin 18.2 aufwiesen. Eine Analyse des FGFR2b-Markers wurde in dieser Studie nicht durchgeführt.19
dMMR = deficient mismatch repair
Claudin 18.2 wird sowohl in Magentumoren vom diffusen als auch vom intestinalen histologischen Typ exprimiert.14

FGFR2b
Der FGFR-Signalweg trägt zur Tumorprogression bei, indem er die Angiogenese und Proliferation vorantreibt.7
Eine Expression von FGFR2b wurde bei 30 % der Adenokarzinome des Magens/AEG beobachtet.20


FGFR2b-Positivität: Überexpression (IHC) und/oder Genamplifikation (ctDNA)
Eine Überexpression von FGFR2b kann mit folgenden Tests detektiert werden15:
HER2
HER2 (human epidermal growth factor receptor 2 ) ist eine Rezeptor-
Tyrosinkinase, die bei einem Adenokarzinom des Magens/AEG überexprimiert und/oder amplifiziert wird.7
HER2 ist ein Protoonkogen, das an Signalwegen beteiligt ist, die zu Zellwachstum und Differenzierung führen.17
Eine HER2-Positivität wurde bei 22 % der fortgeschrittenen Adenokarzinome des Magens/AEG festgestellt.11


HER2-Positivität: Überexpression (IHC3+) und/oder Genamplifikation (FISH positiv)
Der Nachweis einer HER2-Überexpression oder Amplifikation kann mit IHC, ISH-Methoden und NGS erfolgen und ist im Allgemeinen eher mit Tumoren vom intestinalen Typ assoziiert.11,16,17*
*IHC/ISH Testung sollte zuerst in Betracht gezogen werden, gegebenenfalls gefolgt von zusätzlichen NGS-Tests.16
MSI
MSI wird mit genomischer Instabilität und einer erhöhten Wahrscheinlichkeit für die Entwicklung von Tumoren assoziiert.7
Mikrosatelliten sind kurze nicht codierende repetitive Nukleotidsequenzen.12
MSI-H wurde bei 4 % der Adenokarzinome des Magens/AEG beschrieben.23


Der Nachweis von MSI erfolgt in der Regel mit verschiedenen Methoden16:

PD-L1
PD-L1 (programmed death-ligand 1 ) ist ein Oberflächenmolekül, das auf verschiedenen Tumorzellen und/oder Immunzellen exprimiert werden kann.35
Die Expression von PD-L1 wurde in verschiedenen Studien für mehrere CPS-Schwellenwerte analysiert: 67-73 % CPS ≥ 1, 29-31 % CPS ≥ 5 und 16-18 % CPS ≥ 10.21,22*






*Die Daten stammen aus einer randomisierten kontrollierten Studie und einer retrospektiven Real World-Analyse anhand medizinischer Aufzeichnungen.21,22
PD-L1-Expression wird mit IHC detektiert.16
ZUSAMMENFASSUNG
NCCN Clinical Practice Guidelines in Oncology for Gastric Cancer (NCCN Guidelines®) befürworten die Verwendung von Biomarkern zur Verbesserung der Patientenversorgung.16
Die NCCN Guidelines® empfehlen.16
Mit steigender Anzahl entdeckter Biomarker wird eine gezieltere Behandlung des Adenokarzinoms des Magens/AEG möglich.
*IHC/ISH sollte zuerst in Betracht gezogen werden, gegebenenfalls gefolgt von zusätzlichen NGS-Tests.16
Die Biomarker-Forschung erweitert die Sicht auf Patientenpopulationen, liefert Informationen über metastasierte Adenokarzinome des Magens/AEG und trägt wesentlich zur Verbesserung der klinischen Entscheidungsfindung bei.

Haben Sie Fragen?
Laden Sie hier Informationen über Fortschritte der Biomarker beim Adenokarzinom des Magens/AEG herunter.
Klicken Sie auf den unten stehenden Link, um sich für Updates zu den Fortschritten der Biomarker beim Magenkarzinom zu registrieren.
REFERENZEN
§ 1 Urheberrecht
Der gesamte Inhalt der Webseiten ist geistiges Eigentum der Astellas Pharma GmbH und unterliegt dem Schutz des Urheberrechts. Auch die einzelnen Elemente dieser Website sind urheber- bzw. markenrechtlich geschützt; sie dürfen weder kopiert noch im Ganzen oder in Teilen imitiert werden; dies gilt insbesondere für Marken, Logos, Grafiken, Ton- und Bildbestandteile, die auf dieser Website genutzt werden. Jegliche Veränderung, Vervielfältigung, Verbreitung oder öffentliche Wiedergabe der Webseite sowie Teilen hiervon, gleich welcher Art, ist unzulässig.
Nutzer dürfen den Inhalt dieser Webseiten nur für den eigenen, privaten Bedarf laden, ausdrucken oder kopieren. Ein Hinweis auf das Urheberrecht der Astellas Pharma GmbH muss auf jeder Kopie unserer Publikationen oder Teilen davon enthalten sein.
Außerhalb dieser Nutzungserlaubnis ist der Gebrauch ausdrücklich untersagt. Verstöße werden zivil- und strafrechtlich verfolgt.
§ 2 Kennzeichen
Marken, Titel, Logos: Die erwähnten Markenrechte stehen dem jeweiligen Rechtsinhaber zu. Alle der auf dieser Website genannten Produktnamen sind Marken der Astellas-Unternehmensgruppe, verbundener Unternehmen, Lizenznehmer/-geber oder Joint Venture Partner, gleichgültig, ob sie herausgestellt und mit dem Symbol ® gekennzeichnet sind oder nicht. Der Gebrauch oder Missbrauch dieser eingetragenen Warenzeichen ist ausdrücklich verboten und wird nach geltendem Recht verfolgt. Die Produkte, die auf dieser Website für deutsche Adressaten dargestellt werden, können in anderen Ländern unter unterschiedlichen Marken, Bezeichnungen, Ausstattungen und Stärken im Handel sein. Bei Fragen kontaktieren Sie bitte die Astellas Gesellschaft in Ihrem Land.
§ 3 Haftung
3.1 Die Astellas Pharma GmbH und die mit ihr verbundenen Unternehmen übernehmen keine Gewährleistung und keine Haftung im Zusammenhang mit jeglicher Nutzung dieser Webseite. Insbesondere wird keine Haftung für Schäden, welcher Art auch immer, im Hinblick auf die Vollständigkeit und Richtigkeit der Angaben übernommen. Dies gilt ebenso für mögliche Schäden, die in Zusammenhang mit Downloads jeglicher Datei-Formen von unseren Internetseiten entstehen. Die Nutzer erklären sich damit einverstanden, auf diese Webseite und deren Inhalt auf eigenes Risiko zuzugreifen.
3.2 Das Übermitteln von Informationen zur Anbahnung von Vertragsabschlüssen erfolgt rein unverbindlich und ohne Übernahme einer wie auch immer gearteten Verpflichtung oder Haftung.
3.3 Auf dieser Webseite werden Links zu Internetseiten Dritter angeboten, die diese in eigener Verantwortung erstellt haben und die dazu führen, dass Sie die Website der Astellas Pharma GmbH verlassen. Die Verbindung erfolgt ausschließlich zum Zwecke der Information und als zusätzlicher Service für die Nutzer. Die dort erstellten Inhalte stehen in keinerlei Zusammenhang mit unserem Unternehmen. Für Schäden, die aus der Nutzung der Inhalte dieser Seite entstehen, übernehmen die Astellas Pharma GmbH und die mit ihr verbundenen Unternehmen keine Haftung.
§ 4 Einverständniserklärung
Mit der Nutzung/Öffnung der vorliegenden Webseiten erklärt der Nutzer sein Einverständnis mit den hier formulierten Bedingungen. Gleichzeitig erklärt er sich mit der Auswertung seines Zugriffs zu rein statistischen Zwecken einverstanden. Die Nutzung ist zu unterlassen, wenn den Nutzungsbedingungen nicht zugestimmt wird.
§ 5 Adressaten von www.astellas.com/de und Geltungsbereich
Diese Website richtet sich ausschließlich an Adressaten im Gebiet der Bundesrepublik Deutschland.
Soweit die Webseiten Dokumente zu pharmazeutischen Präparaten enthalten, wird dadurch keine Alternative zur Beratung durch einen Arzt oder Apotheker angeboten. Sollten Sie Rat zu spezifischen Gesundheitsproblemen suchen, wenden Sie sich bitte ausschließlich an Ihren Arzt.
Bestimmte Informationen über verschreibungspflichtige Arzneimittel dürfen wir Ihnen nur dann zugänglich machen, wenn Sie gemäß §10 Heilmittelwerbegesetz den medizinischen Fachkreisen angehören.